Применение щелочных металлов 9 класс кратко
Применение щелочных металлов в первую очередь зависит от их химических свойств. Даже в малом количестве все они химически активны, а франций – радиоактивен.
Щелочные металлы – группа небольшая и со сходными физическими свойствами:
- небольшой удельный вес, мягкость (можно мять руками и резать ножом),
- с белым металлическим цветом (кроме цезия),
- предельно низкая температурой плавления (у цезия – всего 28,4 градуса).
Применение щелочных металлов в разных отраслях современной деятельности человека в первую очередь связана с их активностью при вступлении в реакцию с другими веществами.
Практически все они в чистом виде бурно реагируют при контакте с водой, с различными кислотами и кислородом, а также имеют восстановительные свойства.
Учитывая активность материалов щелочного ряда периодической таблицы, все работы с ними должны производиться с максимальной осторожностью, а остатки по завершению ликвидированы.
Широкий спектр возможностей – с щелочными металлами
Щелочные металлы используются во многих отраслях современной промышленности, причём практически всегда в соединении с другими веществами.
Наиболее известное применение щелочных металлов – создание активных щелочных растворов в воде или других жидкостях.
Такие вещества используются в химической промышленности для восстановительных реакций, в процесс изготовления автомобильных шин.

Применение щелочных металлов в машиностроении
В чистом виде натрий, например, служит катализатором при изготовлении каучука, в процессе производства других металлов (титана, циркония, тантала), а его пары – в люминесцентных лампах.
Наиболее известное соединения натрия – это поваренная соль (хлорид натрия), используемое повсеместно.
Литий – один из основных материалов в изготовлении аккумуляторных батарей, а как легирующий материал к алюминию – в авиационной промышленности.
Распространено применение щелочных металлов в процессе изготовления стекла и жидкого мыла, в качестве минерального удобрения и в военной промышленности как взрывчатое вещество.

Наиболее активными среди металлов являются щелочные металлы. Они активно вступают в реакции с простыми и сложными веществами.
Общие сведения
Щелочные металлы находятся в I группе периодической таблицы Менделеева. Это мягкие одновалентные металлы серо-серебристого цвета с небольшой температурой плавления и невысокой плотностью. Проявляют единственную степень окисления +1, являясь восстановителями. Электронная конфигурация – ns 1 .

Рис. 1. Натрий и литий.
Общая характеристика металлов I группы приведена в таблице.
Список щелочных металлов
Активные металлы быстро реагируют с другими веществами, поэтому в природе находятся только в составе минералов.
Получение
Для получения чистого щелочного металла используется несколько способов:
электролиз расплавов, чаще всего хлоридов или гидроксидов –
прокаливание соды (карбоната натрия) с углём для получения натрия –
восстановление кальцием рубидия из хлорида при высоких температурах –
Взаимодействие
Свойства щелочных металлов обусловлены их строением. Находясь в первой группе периодической таблицы, они имеют всего один валентный электрон на внешнем энергетическом уровне. Единственный электрон легко переходит к атому окислителя, что способствует быстрому вступлению в реакцию.
Металлические свойства увеличиваются в таблице сверху вниз, поэтому литий расстаётся с валентным электроном труднее, чем франций. Литий – наиболее твёрдый элемент среди всех щелочных металлов. Реакция лития с кислородом проходит только под воздействием высокой температуры. С водой литий реагирует значительно медленнее, чем остальные металлы группы.
Общие химические свойства представлены в таблице.
Оксид (R2O) образует только литий. Натрий образует смесь оксида и пероксида (R2O2). Остальные металлы образуют надпероксиды (RO2)
2Na + 2HCl → 2NaCl + H2↑
С азотом (реагирует только литий при комнатной температуре)
С углеродом (реагируют только литий и натрий)
При качественной реакции имеют разный цвет пламени. Литий горит малиновым, натрий – жёлтым, цезий – розово-фиолетовым пламенем. Оксиды щелочных металлов также имеют разный цвет. Натрий становится белым, рубидий и калий – жёлтыми.

Рис. 2. Качественная реакция щелочных металлов.
Применение
Простые металлы и их соединения используются для изготовления лёгких сплавов, металлических деталей, удобрений, соды и других веществ. Рубидий и калий используются в качестве катализаторов. Пары натрия применяются в люминесцентных лампах. Не имеет практического применения только франций из-за радиоактивных свойств. Как используют элементы I группы кратко описано в таблице применения щелочных металлов.
– Натрий ускоряет реакцию при производстве каучука;
– гидроксид калия и натрия – производство мыла;
– карбонат натрия и калия – изготовление стекла, мыла;
– гидроксид натрия – изготовление бумаги, мыла, ткани;
– нитрат калия – производство удобрений
– Хлорид натрия – поваренная соль;
– гидрокарбонат натрия – питьевая сода
Калий и натрий являются восстановителями при получении титана, циркония, урана
– Расплавы калия и натрия используются в атомных реакторах и авиационных двигателях;
– литий используется для производства аккумуляторов
Цезий – производство фотоэлементов
Авиация и космонавтика
Сплавы из алюминия и лития используются для корпусов машин и ракет

Рис. 3. Питьевая сода.
Что мы узнали?
Из урока 9 класса узнали об особенностях щелочных металлов. Они находятся в I группе таблицы Менделеева и при реакциях отдают один валентный электрон. Это мягкие металлы, легко вступающие в химические реакции с простыми и сложными веществами – галогенами, неметаллами, кислотами, водой. В природе встречаются только в составе других веществ, поэтому для их извлечения используется электролиз или реакция восстановления. Применяются в промышленности, строительстве, металлургии, энергетике.
Щелочные металлы — группа неорганических веществ, простых элементов таблицы Менделеева. Все они обладают похожим атомным строением и соответственно, похожими свойствами. В группу входят калий, натрий, литий, цезий, рубидий, франций и теоретически описанный, но еще не синтезированный элемент унуне́нний. Первые пять веществ существуют в природе, франций — искусственно созданный, радиоактивный элемент. Свое название щелочные металлы получили из-за способности образовывать щелочи в реакции с водой.
Вся элементы группы химически активны, поэтому на Земле встречаются только в составе различных минералов, например, каменной, калийной, поваренной соли, буры, полевого шпата, морской воды, подземных рассолов, чилийской селитры. Франций часто сопутствует урановым рудам; рубидий и цезий — минералам с натрием и калием.
Свойства
Активность в группе увеличивается по мере роста атомной массы: Li →Cs. Обладают восстановительными свойствами, в том числе в реакции с водородом. Проявляют валентность -1. Бурно реагируют с водой (все кроме лития — со взрывом); с кислотами, кислородом. Взаимодействуют с неметаллами, спиртами, водным аммиаком и его производными, карбоновыми кислотами, многими металлами.
Калий и натрий являются биогенными элементами, участвуют в водно-солевом и кислотно-щелочном балансе человеческого организма, необходимы для нормальной циркуляции крови и функционирования многих энзимов. Калий важен для растений.
В нашем организме есть и рубидий. Его нашли в крови, костях, головном мозге, легких. Он оказывает противовоспалительное, противоаллергическое действие, притормаживает реакции нервной системы, усиливает иммунитет, положительно влияет на состав крови.
Меры предосторожности
Щелочные металлы очень опасны, способны воспламеняться и взрываться просто от контакта с водой или воздухом. Многие реакции протекают бурно, поэтому работать с ними допускается только после тщательного инструктажа, с применением всех мер предосторожностей, в защитной маске и защитных очках.
Растворы калия, натрия и лития в воде являются сильными щелочами (гидроксиды калия, натрия, лития); контакт с кожей приводит к глубоким болезненным ожогам. Попадание щелочей, даже низкой концентрации, в глаза может привести к слепоте. Реакции с кислотами, аммиаком, спиртами проходят с выделением пожаро- и взрывоопасного водорода.
Щелочные металлы хранят под слоем керосина или вазелина в герметичных емкостях. Манипуляции с чистыми реактивами проводят в аргоновой атмосфере.
Следует тщательно следить за утилизацией остатков после опытов со щелочными металлами. Все остатки металлов предварительно должны быть нейтрализованы.
Применение
- Цезий и рубидий используются в фотоэлементах, топливных элементах.
- Цезий применяется в источниках тока, энергоемких аккумуляторах, счетчиках радиоактивных частиц, гамма-спектрометрах для космических аппаратов; приборах ночного видения и оружейных прицелах. Изотопы цезия используются для стерилизации пищевой тары, медицинских инструментов, мясных продуктов, лекарств; они входят в состав некоторых лекарств, применяются для радиотерапии опухолей.
- Рубидий входит в состав болеутоляющих, снотворных, успокаивающих препаратов. Применяется в телевизионных трубках, оптических приборах, низкотемпературных источниках тока, в смазке для космических аппаратов, высокочувствительных магнитометрах для космических и геофизических исследований. Производные рубидия используются в атомной промышленности, химпроме, вакуумных радиолампах, высокотемпературных термометрах.
- Калий и натрий применяются в воздухо-восстановительных системах на подводных лодках и батискафах, в автономных противогазах и дыхательных аппаратах.
- Литий востребован в источниках тока, для производства подшипниковых сплавов и литийорганических соединений, как катализатор в химпроме.
- Натрий применяется в газоразрядных лампах, в металлургии; как теплоноситель в атомной индустрии; в химической индустрии в процессах орг.синтеза.
- В разных сферах промышленности и быта используется большое количество производных щелочных металлов, например, пищевая и кальцинированная сода, поваренная соль, натриевая и калийная селитра, нитраты, сульфаты, карбонаты, гидроксиды натрия, калия и лития и пр.
Наиболее активными среди металлов являются щелочные металлы. Они активно вступают в реакции с простыми и сложными веществами.

Общие сведения
Щелочные металлы находятся в I группе периодической таблицы Менделеева. Это мягкие одновалентные металлы серо-серебристого цвета с небольшой температурой плавления и невысокой плотностью. Проявляют единственную степень окисления +1, являясь восстановителями. Электронная конфигурация – ns1.

Рис. 1. Натрий и литий.
Общая характеристика металлов I группы приведена в таблице.
Список щелочных металлов
Активные металлы быстро реагируют с другими веществами, поэтому в природе находятся только в составе минералов.
Получение
Для получения чистого щелочного металла используется несколько способов:
электролиз расплавов, чаще всего хлоридов или гидроксидов –
прокаливание соды (карбоната натрия) с углём для получения натрия –
восстановление кальцием рубидия из хлорида при высоких температурах –
Взаимодействие
Свойства щелочных металлов обусловлены их строением. Находясь в первой группе периодической таблицы, они имеют всего один валентный электрон на внешнем энергетическом уровне. Единственный электрон легко переходит к атому окислителя, что способствует быстрому вступлению в реакцию.
Металлические свойства увеличиваются в таблице сверху вниз, поэтому литий расстаётся с валентным электроном труднее, чем франций. Литий – наиболее твёрдый элемент среди всех щелочных металлов. Реакция лития с кислородом проходит только под воздействием высокой температуры. С водой литий реагирует значительно медленнее, чем остальные металлы группы.
Общие химические свойства представлены в таблице.
Оксид (R2O) образует только литий. Натрий образует смесь оксида и пероксида (R2O2). Остальные металлы образуют надпероксиды (RO2)
Читайте также:
- Период судей в ветхом завете кратко
- Шульгин василий витальевич биография кратко
- Сверхъестественное кратко 11 сезон
- Гроза место действия своеобразие конфликта кратко
- Дальневосточная кампания советской армии кратко
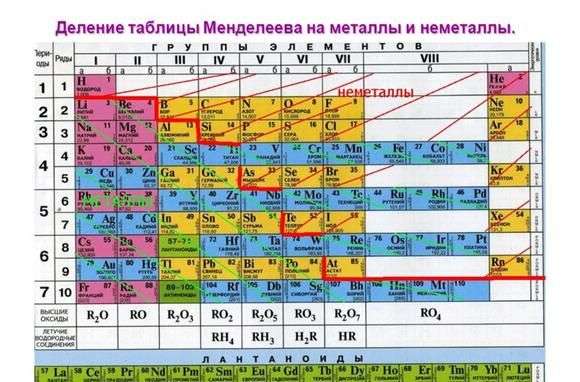
Металл легко вступающий в соединение с людьми

- щелочные металлы (элементы подгруппы Ia, кроме водорода),
- щелочно-земельные металлы (Ca, Sr, Ba, Ra — элементы подгруппы IIa),
- алюминий — элемент подгруппы IIIa.
Щелочные и щелочно-земельные металлы получили свое название благодаря тому, что их гидроксиды растворяются в воде, то есть являются щелочами.
Электронное строение активных металлов характеризуется наличием на внешней электронной оболочке одного, двух или трех электронов, относительно слабо связанных с ядром. В результате химических реакций металлы легко отдают эти электроны, проявляя свои постоянные степени окисления и валентности:
степень окисления +1
валентность I
степень окисления +2
валентность II
степень окисления +3
валентность III
Благодаря своей активности щелочные и щелочно-земельные металлы, равно как и алюминий, встречаются в природе не в чистом виде, а в составе многочисленных химических соединений — минералов. Минералы представляют собой кристаллические вещества, как правило оксиды или соли. У многих из них в кристаллической решетке содержатся молекулы воды: такие соединения называются кристаллогидратами. Например в глаубе́ровой соли на один фрагмент сульфата натрия приходится десять молекул воды; он имеет формулу и название декагидрат сульфата натрия (по-гречески дека — десять).
Самородный кристалл галита (NaCl)
Original by Rob Lavinsky , iRocks.com
- CaCO3 — кальцит, основной компонент мела и мрамора (рис. 2),
- CaSO4·2H2O — гипс,
- CaF2 — флюорит,
- BaSO4 — барит.
Различные модификации кальцита (CaCO3)
Original by Rob Lavinsky , iRocks.com
Основные запасы алюминия сконцентрированы в глинозёмах и полевых шпатах — соединениях кремния, кислорода, алюминия и других металлов, — а также в некоторых минералах: корунде (Al2O3), бокситах (Al2O3·H2O) и др. Алюминий — самый распространенный металл в земной коре.
Получение активных металлов
Промышленное производство алюминия основано на электролизе глинозёмов в расплаве криолита (Na3AlF6).
Химические свойства активных металлов
а калий, рубидий и цезий — надпероксиды, или супероксиды:
Щелочно-земельные металлы и алюминий также образуют оксиды; при комнатной температуре их поверхность покрывается оксидной пленкой, при нагревании происходит интенсивное самовозгорание:
Так, посуда, провода, детали машин и механизмов и прочие изделия из алюминия покрыты тонкой пленкой Al2O3. Эта пленка не пропускает ни воздух, ни влагу, предотвращая тем самым дальнейшее окисление металла, иначе срок службы алюминиевых изделий не превышал бы нескольких минут. Однако, если потравить (т. е. обработать химически агрессивной средой) поверхность такого изделия, то несколько мгновений можно будет наблюдать характерный блеск чистого алюминия (рис. 3).
Поверхность алюминиевого бруска после травления
Original by Alchemist-hp
Исключением является реакция алюминия с водородом, которая не идет даже при нагревании.
Видеоролик поочередно демонстрирует взаимодействие лития, натрия, калия, рубидия и цезия с водой. Можно заметить, что в этом ряду активность металлов возрастает
На английском языке
Однако, следует иметь в виду, что если щелочной или щелочно-земельный металл попадет в разбавленный раствор кислоты, то начинают протекать две конкурирующие реакции — с кислотой и водой:
Образующаяся в результате второй реакции щелочь впоследствии также вступает во взаимодействие с кислотой; в итоге все равно образуется нейтральное соединение — соль:
Такие металлургические процессы, сопровождающиеся обычно выделением большого количества тепла, объединяют под общим названием металлотермия.
Воспламенение термитной смеси (смеси порошков алюминия и оксида железа)
Original by Schuyler S.
Применение активных металлов и их соединений
Упомянутая выше металлотермия — основная область применения всех активных металлов, которые являются отличными восстановителями.
Щелочные металлы имеют высокую теплопроводность, но в то же время достаточно низкую температуру плавления (натрий — +98 °С, калий — +64 °С). Эти свойства обуславливают применение щелочных металлов и их сплавов в качестве эффективных теплоносителей, например в атомных реакторах.
Небольшие добавки щелочных и щелочно-земельных металлов в сплавы алюминия, меди, свинца придают им пластичность и стойкость к коррозии.
Газоразрядные лампы, заполненные пара́ми натрия, дают яркий желто-оранжевый свет и широко применяются в уличном освещении (рис. 5).
Характерный свет фонарей с натриевыми газоразрядными лампами. Сеул, Республика Корея
Original by d’n’c on flickr.com
Среди соединений щелочных и щелочно-земельных металлов наибольшее применение находят непосредственно щелочи, а также оксиды, фториды, хлориды, карбонаты и некоторые другие. Гидроксиды лития, натрия и калия используются для приготовления электролитов щелочных батарей, а оксид лития — один из основных компонентов литий-ионных аккумуляторов, которыми снабжаются большинство современных сотовых телефонов, ноутбуков, цифровых фотоаппаратов и других мобильных устройств.
Фториды кальция и бария применяются в изготовлении оптических приборов — объективов, линз и призм.
Неорганические соединения калия и кальция (K2CO3, KNO3, Ca(OH)2 и др.) широко используются в качестве минеральных удобрений.
Алюминий и его сплавы — легкие, прочные и коррозионно-устойчивые, — применяются для изготовления корпусов всевозможных механизмов (рис. 6), деталей электронных устройств, проводов, посуды и пр.
Сплавы алюминия — основной материал для изготовления корпусов воздушных судов
Original by Caribb on flickr.com
Непосредственно алюминий и некоторые его соединения, в том числе органические, используются в качестве высокоэффективного ракетного топлива.
2. Закончите уравнения реакций:
| Al + CuO → . Na + ZnCl2 → . Ca + S → . | Li + H2O → . Al + H2SO3→ . Cs O2 + Cs → . |
 |
| 4Al + 6CuO → 6Cu + 2Al2O3 2Na + ZnCl2 → Zn + 2NaCl Ca + S → CaS | 2Li + 2H2O → 2LiOH + H2 2Al + 3H2SO3→ Al2(SO3)3 + 3H2 Cs O2 + 3Cs → 2Cs2O |
Металлы IA группы
Эти металлы — очень активные! Именно их кидают в ванны с водой, в результате чего происходят мощщные взрывы.
Щелочные металлы
IA группа называется главной подгруппой первой группы, в которую входят щелочные металлы: литий Li, натрий Na, калий K, рубидий Rb, цезий Cs и франций Fr.
Щелочные металлы — серебристо-белые металлы с высокой электро- и теплопроводностью, обладают ковкостью, пластичностью и металлическим блеском.
Главная особенность строения атомов химических элементов IA группы заключается в том, что они содержат один электрон на внешнем энергетическом уровне — их электронная конфигурация ns 1 .
Из этого следует, что атомам щелочных металлов энергетически выгодно отдать электрон и приобрести конфигурацию инертного газа, приобретая при этом степень окисления +1.
Основным способом получения таких металлов является электролиз расплавов солей.
Химические свойства
Их химические свойства крайне логичны:
- как типичные металлы они будут вступать в реакции со своими противоположностями — неметаллами;
- как восстановители — реагировать с окислителями (в том числе восстанавливать металлы и неметаллы из их оксидов);
- как металлы, стоящие в ряду активности до водорода — вступать в реакции вытеснения с водой, кислотами-неокислителями и солями менее активных металлов.
- Реакции с неметаллами
Как типичные восстановители, щелочные металлы могут взаимодействовать со своими противоположностями — неметаллами.
| Гидриды металлов подвергаются необратимому гидролизу |
В реакциях с щелочными металлами кислород образует ряд веществ:
- литий («кандидат от народа»), как и подавляющее большинство металлов, образует оксид;
4Li + O2 = 2Li2O - натрий образует пероксид;
2Na + O2 = Na2O2 - калий и все нижестоящие металлы — надпероксиды/супероксиды.
K + O2 = KO2
- Реакции с водой
В ряду активности щелочные металлы находятся до водорода, поэтому они способны вытеснять водород из воды:
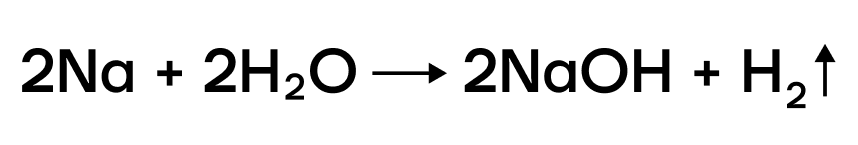
Можно представить воду как HOH, тогда металл (например, натрий) будет замещать один из атомов водорода с образованием NaOH.
За счет крайне низких значений электроотрицательности металлы очень слабо притягивают к себе электроны, а следовательно, у них «легко их украсть». Делаем вывод: в ОВР щелочные металлы проявляют ярко выраженные восстановительные свойства, повышая в реакциях степени окисления.
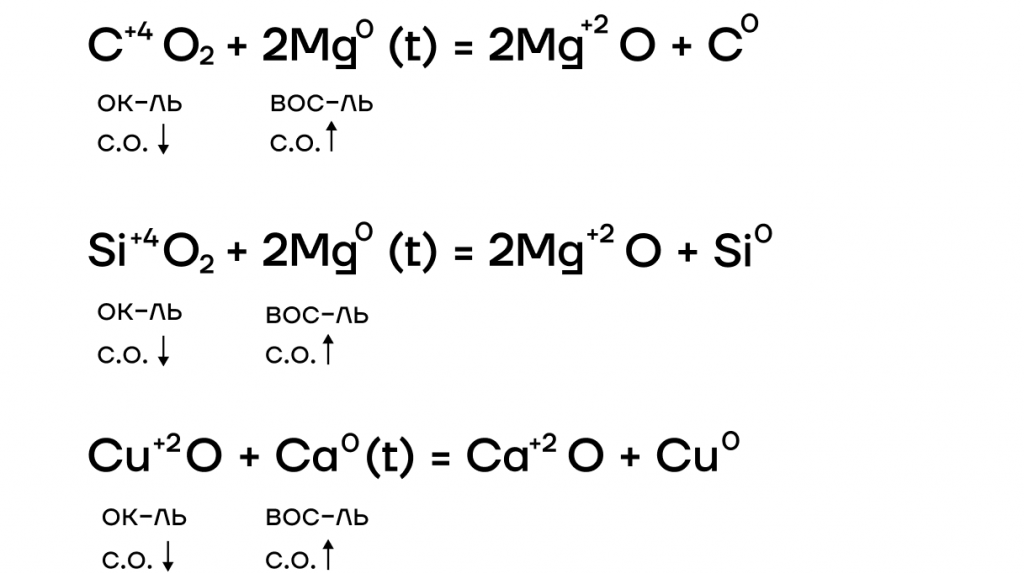
Оксиды щелочных металлов
По физическим свойствам это — бесцветные кристаллические вещества, хорошо растворимые в воде.
Они являются основными оксидами, поэтому:
- реагируют с водой с образованием оснований:

- вступают в основно-кислотные взаимодействия со своими противоположностями, обладающими кислотными свойствами: кислотами, кислотными оксидами, амфотерными оксидами и гидроксидами:
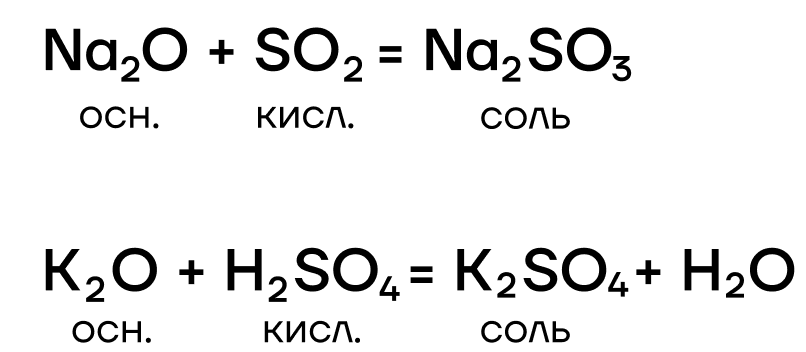
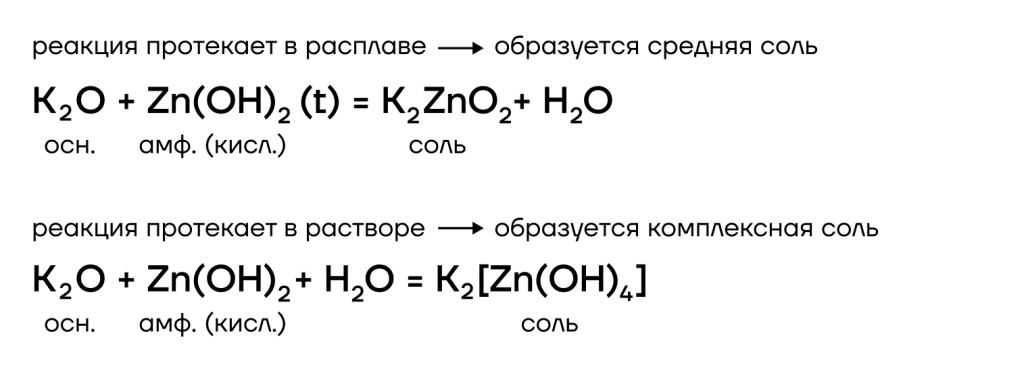
Гидроксиды щелочных металлов
Что же это такое? По-другому их называют щелочами. Они представляют собой бесцветные кристаллические вещества, хорошо растворимые в воде.
По химическим свойствам они являются типичными сильными основаниями, то есть:
- диссоциируют в растворах с образованием гидроксид-анионов. создавая в растворах щелочную среду:
- вступают в основно-кислотные взаимодействия со своими противоположностями (кислотами и кислотными оксидами + амфотерные оксиды и гидроксиды), образуя соли;
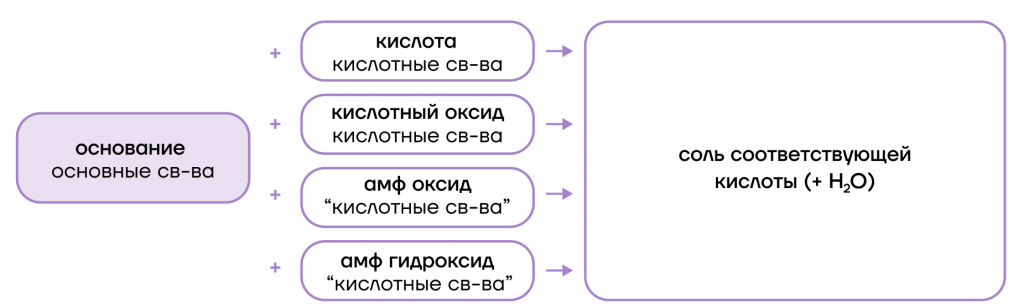
- вступают в реакции ионного обмена с кислотами и солями:
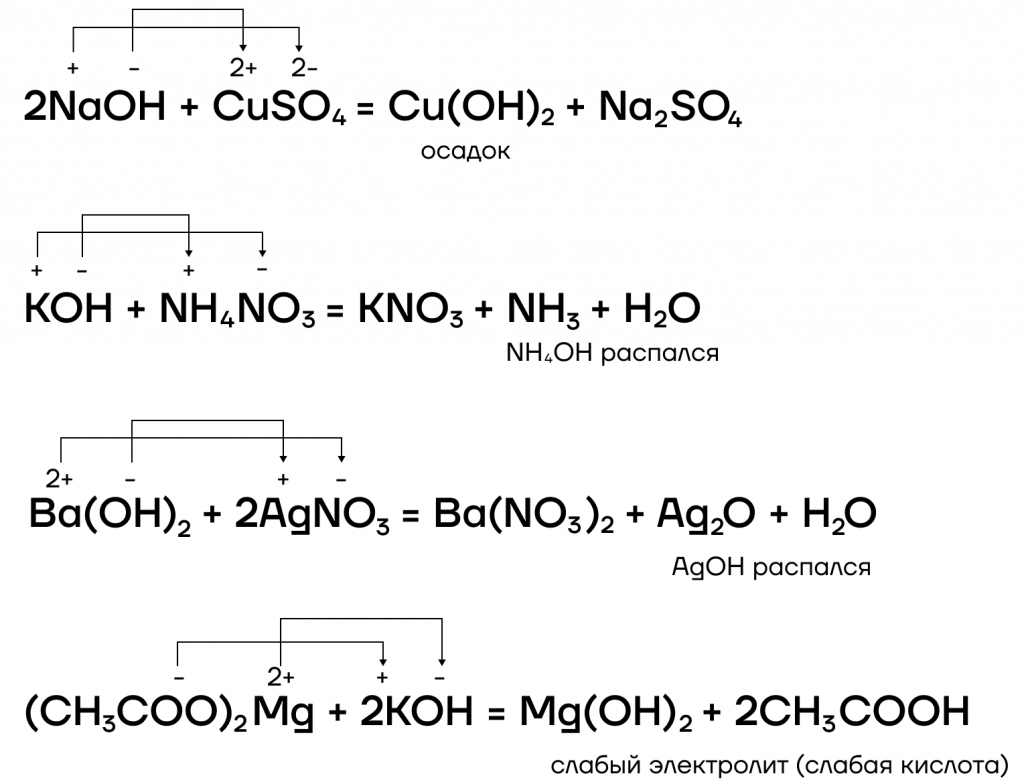
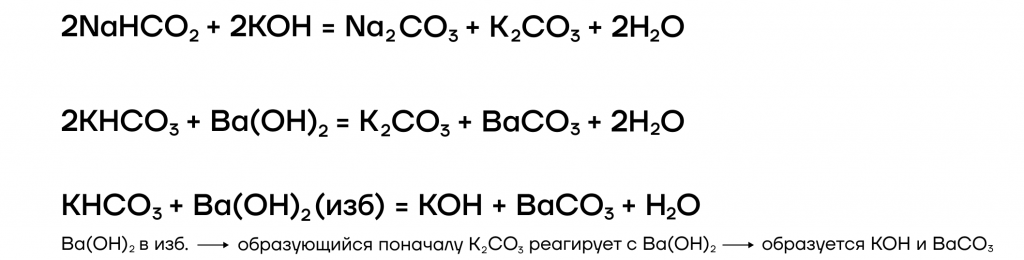
Какие же специфические свойства щелочей существуют? Рассмотрим некоторые из них:
- Окислительно-восстановительные реакции с металлами
Из металлов со щелочами напрямую взаимодействуют только амфотерные бериллий Be, цинк Zn, алюминий Al.
| Эти металлы можно запомнить по аббревиатуре BeZnAl |
А какие соли тогда будут образовываться? В растворе образуются комплексные соли, а в расплаве (t) — средние. В качестве еще одного продукта реакции выделяется газообразный водород.
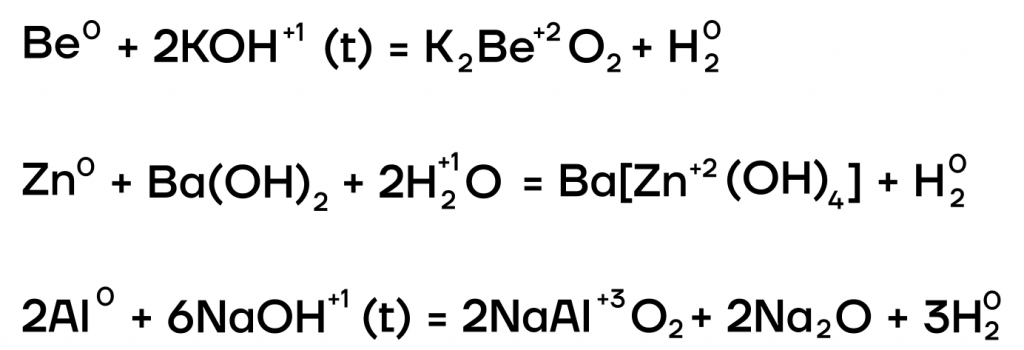
- Окислительно-восстановительные реакции с неметаллами
Неметаллы, которые могут реагировать со щелочами, можно запомнить по «крестообразному» расположению в таблице Менделеева:

Пероксиды щелочных металлов
Что же такое пероксиды? Пероксиды — сложные вещества, которые содержат группу —О—О—, где кислород имеет степень окисления −1.
Фактчек
- Металлы IA группы называются щелочными металлами, которые представлены литием, натрием, калием, рубидием, цезием и францием.
- Постоянная валентность щелочных металлов I, постоянная степень окисления — +1.
- Основной способ получения щелочных металлов — электролиз расплавов солей.
- Щелочные металлы — чрезвычайно активные металлы, могут реагировать с большим рядом простых веществ, с водой.
Проверь себя
Задание 1.
Какой из щелочных металлов имеет самое большое число электронов?
Задание 2.
Щелочные металлы имеют постоянную степень окисления:
Задание 3.
Щелочные металлы образуют с серой соединения, называемые:
- Сульфиты;
- Сульфиды;
- Сульфаты;
- Сульфонаты.
Задание 4.
При реакции калия с кислородом образуется:
- Оксид калия;
- Пероксид калия;
- Супероксид калия;
- Озонид калия
Задание 5.
При внесении солей натрия в пламя оно приобретает окраску:
- Фиолетовую;
- Желтую;
- Небесно-голубую;
- Малиновую
Ответы: 1. — 6; 2. — 1; 3. — 2; 4. — 3; 5. — 2.
Источник https://obrazovanie-gid.ru/pereskazy1/primenenie-schelochnyh-metallov-9-klass-kratko.html
Источник https://nscience.ru/chemistry/inorganic/active_metals/
Источник https://umschool.net/library/himiya/metally-ia-gruppy/